Manual de analítica
Es para mi un gran placer el poder presentar esta edición digital del LabPocket BOOK: un sencillo y práctico manual de bolsillo de análisis de laboratorio veterinario de pequeños animales LabPocket BOOK es fruto de la experiencia de más de 30 años de análisis clínicos veterinarios y pretende facilitar la labor diaria del veterinario clínico de pequeños animales.
Esta edición resumida, está pensada para que pueda ser consultada en cualquierlugar y desde cualquier dispositivo, en todo momento. La información que hemos recopilado ha sido presentada de un modo muy sistemático y sintético para facilitar la rápida consulta del manual.
El análisis clínico es esencial, dentro de la primera fase del diagnóstico veterinario en su proceso y abordaje del caso. Un buen diagnóstico es crítico para la prescripción del tratamiento posterior y puede conseguir una rápida mejora del bienestar de nuestros pacientes, los perros y los gatos.
Esta edición en formato digital se actualiza periódicamente, y puede encontrarse en el apartado LABPOCKET dentro del menú de la única web especializada en medicina interna en Español, https://www.affinity-petcare.com/veterinary/.
Esta edición especial está divida en 4 secciones:
I) Sección dedicada a las nociones más básicas del manejo de las muestras, ya que debemos recordar que un resultado de laboratorio puede ser tan bueno como buena es la muestra que se analiza.
II) Abarca una serie de protocolos dinámicos de diagnóstico tanto bioquímicos como hormonales.
III) Encontramos la Guías de Interpretación Rápida, que de una forma rápida y concreta nos dan una primera idea en la interpretación de los resultados.
IV) Información sobre las principales interferencias analíticas, tablas de conversión de unidades y valores de referencia de los parámetros más utilizados.
Esperamos que sea de vuestro agrado.

Jaume Rodón
Veterinario
Diplomado en Hematología y Bioquímica animal
Diplomado en gestión de información científica
Pasamos a detallar los aspectos más básicos del manejo de muestras.
OBTENCIÓN DE LA MUESTRA
Realizar una venipunción clara y limpia evitando "explorar" con la aguja (fundamental para minimizar hemólisis y coagulación no deseada)
El uso de una presión negativa excesiva puede producir bien un colapso del vaso o bien una paso demasiado rápido de los hematíes a través de la aguja.
Quitar la aguja de la jeringa y transferir la sangre al tubo/s adecuado/s sin ejercer una presión excesiva.
PROCESAMIENTO Y CONSERVACIÓN DE LA MUESTRA
Incluye el período comprendido entre la obtención de la muestra y su análisis en el laboratorio.
1.SUERO
Aunque en cada técnica se indica el tipo de muestra requerido, el suero es la muestra de elección por defecto (excepto en hematología y coagulación) ya que resulta fácil de obtener y de procesar, y no existe ninguna interferencia por el anticoagulante.
Obtención
- Recoger la muestra en tubos sin anticoagulante (preferiblemente con activadores de la coagulación)
- Dejar coagular durante 15-30 minutos (mejor dejar que se retraiga el coágulo.
- Centrifugar, separar el suero y ponerlo en un tubo de plástico. Si se prevé un etraso, entre la extracción de la sangre y la separación del suero mayor de dos horas, se recomienda refrigerar la muestra para disminuir el efecto de la hemólisis.
Normalmente por cada 1 cc de sangre entera se pueden obtener 0.3 cc de suero.
- Marcar el tubo, y refrigerar o congelar si no se va a enviar en los próximos 1-3 días.
El envío de muestras de sangre entera coagulada y no separada no es aconsejable, ya que seguramente se producirá una hemólisis grave.
2.PLASMA
Más apropiado en situaciones donde esté indicado un análisis rápido (por ejemplo: urgencias), ya que la preparación del plasma no requiere completar la coagulación antes de la centrifugación.
Habitualmente puede obtenerse un volumen mayor de plasma que de suero, a partir de un volumen dado de sangre entera.
Obtención
- Recoger la sangre en tubos con anticoagulante
Anticoagulantes
EDTA
Es el anticoagulante de elección para realizar hemogramas ya que conserva la morfología celular. Mezclar la sangre por inversión suave durante 1-2 min.
Existe EDTA sódico y EDTA potásico. El EDTA es un quelante de calcio y magnesio y por lo tanto es mejor no usarlo para bioquímica.
Heparina
Proporciona una conservación celular pobre. Puede usarse en la mayoría de bioquímicas.
Citrato
Imprescindible para pruebas de coagulación: Se debe obtener la muestra, centrifugar, separar y refrigerar y/o congelar dependiendo de los requisitos.
Centrifugar dentro de los 15 primeros minutos. Separar el plasma a tubos de plástico sin nada y refrigerar o congelar según se indique.
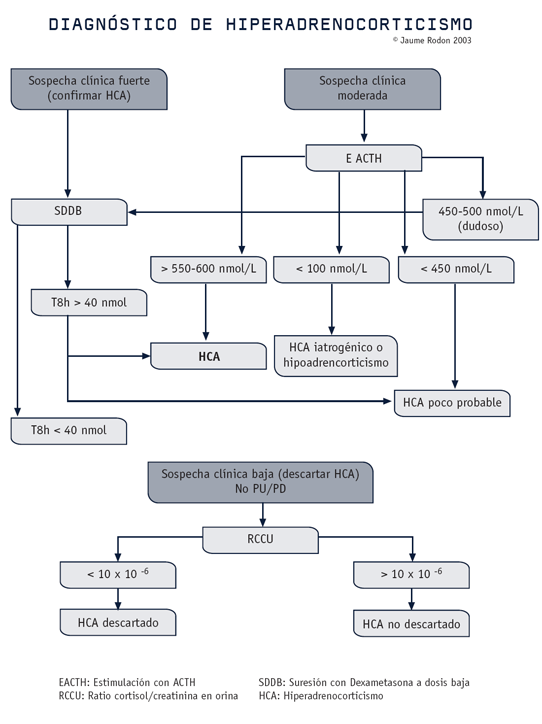
Protocolo de estimulación con ACTH
Indicaciones
Se usa en el diagnóstico de Hiperadrenocorticismo (HAC) e Hipoadrenocorticismo
Protocolo
Extraer sangre del animal (T0) y administrar la ACTH (consultar a VetLab dosis y vía). Volver a sacar sangre a 1 hora (T1). Enviar los sueros separados, bien señalados y refrigerados para la medición de Cortisol.
Interpretación
Los perros normales muestran una aumento de hasta 450 nmol/L (16 mcg/dl) en la muestra post-estímulo. En animales con HAC pituitario dependiente la muestra post-estímulo alcanza valores de 600-1000 nmol/L (22-36 mcg/dl). Los perros con tumores adrenales (TA) tienen valores basales por encima de 260 nmol/L (9,5 mcg/dl) y valores en la muestra post-estímulo sin cambios o poca variación. Este test no es tan sensible para detectar TA y los resultados que no son diagnósticos deberían ser confirmados con un test de supresión con dexametasona a dosis bajas, especialmente en animales con signos de cushing. (Ver algoritmo 1). En perros con hipoadrenocorticismo la muestra post-estímulo no mostrará cambio alguno. La respuesta clásica en animales con enfermedad de Addison son ambos valores < 20 nmol/L (0,7 mcg/dl).
Protocolo de supresión con Dexametasona a dosis baja
Indicaciones
Para confirmar el diagnóstico de un perro muy sospechoso de HAC
Protocolo
Extraer sangre del animal (T0) y administrar 0.01 mg/kg de Dexametasona vía I.V. En animales pequeños es mejor hacer una dilución en 2 cc de suero fisiológico o agua para inyección. Volver a sacar sangre a las 3-4 horas (T1) y a las 8 horas (T2). Enviar los sueros separados, bien señalados y refrigerados para la medición de Cortisol. Los perros normales suprimen sus valores de cortisol en por lo menos el 50% del valor basal en las 3-4 primeras horas, y luego los valores permanecen por debajo de 40 nmol/L (1,4 mcg/dl) a las 8 horas.
Interpretación
Los perros con HAC pituitario dependiente disminuyen los valores de cortisol a las 3-4 horas pero vuelven a aumentar a las 8 horas a valores > 40 nmol/L (1,4 mcg/dl). Los perros con tumor adrenal no disminuyen los valores a las 3 horas y permanecen > 40 nmol/L (1,4 mcg/dl) a las 8 horas (Ver algoritmo 1).
Protocolo de supresión con Dexametasona a dosis alta
Indicaciones
Se usa para distinguir entre HAC de pituitaria o tumor adrenal. Debe usarse después de que el test a dosis baja ha confirmado la presencia del HAC.
Protocolo
Extraer sangre del animal (T0) y administrar 0.1-1 mg/kg de Dexametasona vía I.V. Volver a sacar sangre a las 4 horas (T1) y a las 8 horas (T2). Enviar los sueros separados, bien señalados y refrigerados para la medición de Cortisol.
Interpretación
Los perros con tumores adrenales tienen una supresión menor del 50% del valor basal en ambas determinaciones
Protocolo de supresión con Dexametasona en orina
Indicaciones
Diagnóstico de HAC en perros fácilmente estresables.
Protocolo
Se toma una primera muestra de orina la mañana del primer día. La mañana del segundo día se toma la segunda muestra de orina y seguidamente se administra al perro 0,1 mg/kg de dexametasona vía oral. A las 8 horas se administra la segunda dosis de dexametasona. A las 16 horas se administra la 3ª dosis de dexametasona. A la mañana siguiente (tercer día) se toma la tercera muestra de orina. Todas las muestras deben mantenerse refrigeradas. Enviar las orinas, bien señaladas y refrigeradas para la medición del ratio cortisol:creatinina.
Interpretación
Los perros normales tienen ratios menores de 10 x 106. Se sospecha de HAC cuando el ratio es > 30 x 106 en las dos primeras muestras consecutivas. Si en la 3ª muestra el valor disminuye el 50% de la media de las dos primeras muestras es compatible con HAC pituitario dependiente. Si la disminución es menos del 50%, se debería realizar una ACTH endógena para investigar la existencia un tumor adrenal.
Protocolo combinado de estimulación de ACTH con supresión con Dexametasona
Indicaciones
Diagnóstico de HAC en casos dudosos.
Protocolo
Extraer sangre del animal (T0) y administrar dexametasona a dosis de 0.1 mg/kg vía IV. Volver a sacar sangre del animal a 4 horas (T1) y administrar la ACTH como en una estimulación normal (la muestra postdexametasona a las 4 horas sirve como la basal para la estimulación con ACTH) y sacar sangre en 1 hora (T2). Enviar los sueros separados, bien señalados y refrigerados para la medición de Cortisol.
Interpretación
Junta las ventajas e inconvenientes de los dos protocolos.
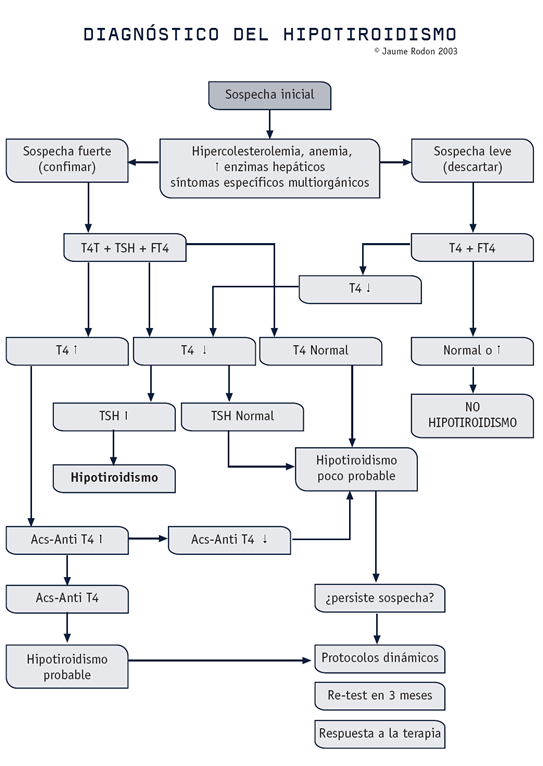
Protocolo de estimulación con TSH
Indicaciones
Diagnóstico de hipotiroidismo canino en perros con síndrome del eutiroideo enfermo.
Protocolo
Extraer sangre del animal (T0) y administrar 75 mcg de TSH (Thyrogen) por perro. Volver a sacar sangre a las 4 horas (T1). Enviar los sueros separados, bien señalados y refrigerados para la medición de T4.
Interpretación
Un perro normal debe aumentar sus valores basales x 1,5 ó x 2 y/o alcanzar una concentración de 26 nmol/L (2 mcg/dl) (ver algortimo 2).
Protocolo de estimulación con TRH
Indicaciones
Diagnóstico de hipotiroidismo canino en perros con valores de T4 dudosos e investigación del hipotiroidismo secundario.
Protocolo
Extraer la sangre del animal (T0). Administrar la TRH, vía IV lenta, a razón de 100 mcg para animales de 1-5 kg, 200 mcg para animales de 5-30 kg y 300 mcg para animales > 30 kg. Se toma una segunda muestra a las 4 -6 horas. Enviar los sueros separados, bien señalados y refrigerados para la medición de T4 y/o TSH.
Interpretación
En animales normales los niveles de T4 deben aumentar x 1,2 la concentración basal o alcanzar un valor de 25 nmol/L (2 mcg/dl). Si la muestra preestimulación es > 25 nmol/L (2 mcg/dl) el animal es normal, independientemente del valor post-TRH. A veces se observan valores basales normales/altos que no estimulan x 1,2 veces. Posiblemente en estos perros la glándula está estimulada al máximo y no puede responder más. Este protocolo es útil en el diagnóstico de hipotiroidismo secundario midiendo la TSH basal y la TSH a los 30 minutos post TRH. Los perros normales deben aumentar su TSH por lo menos en 0,4 ng/ml. (ver algortimo 2)
Protocolo de T4 Post-pill
Indicaciones
Monitorización del tratamiento de hipotiroidismo. Se debe empezar la monitorización un mes después de empezar el tratamiento.
Protocolo
Extraer sangre del animal antes de la medicación (T0) y otra muestra a las 6 horas (T1) si el animal recibe 2 tomas al día o a las 6 horas (T0) y a las 24 horas (T1) si el animal recibe una toma al día. Enviar los sueros separados, bien señalados y refrigerados para la medición de T4.
Interpretación
Los valores no deben ser menores de 37 nmol/l (2,9 mcg/dl) o dentro del intervalo de referencia.
Protocolo de supresión con T3 en gatos
Indicaciones
En la mayoría de casos el diagnóstico del hipertiroidismo felino se consigue midiendo T3, T4 y/o T4 libre en una única muestra basal. En casos donde hay una sospecha clínica de hipertiroidismo pero estas hormonas tiroideas están normales se puede utilizar este test de supresión.
Protocolo
Extraer una muestra de sangre dejar coagular, separar el suero y congelar (T0). Administrar 25 mcg de T3 cada 8 horas durante 2 días; administrar la séptima dosis la mañana del tercer día. Extraer otra muestra de sangre 2-4 horas después de la última dosis (T1). Todas las muestras deben mantenerse refrigeradas. Enviar los sueros separados, bien señalados y refrigerados para la medición de T3 y T4 en ambas muestras.
Interpretación
Un reducción de T4 en T1 > 50% indica un gato normal y/o una enfermedad no tiroidea. Una reducción < 50% pero > 35% sugiere un gato normal y/o una enfermedad no tiroidea. Una reducción < 35% sugiere un gato hipertiroideo. Los valores de T3 deben estar por encima del valor normal, indicando que la administración de T3 ha sido efectiva.
Protocolo de detección de la ovulación en la hembra con la determinación de progesterona
Indicaciones
Se usan determinaciones seriadas de progesterona después del inicio de la hemorragia vaginal para determinar el mejor momento de la monta. Es útil en hembras con disminución de la fertilidad en general.
Protocolo
Se toma una muestra sanguínea a los 7 días del inicio de la hemorragia vaginal. En la mayoría de hembras la concentración de progesterona será < 3nmol/L indicando que la ovulación todavía no ha ocurrido. Si los niveles de progesterona están por encima de 6 nmol/L la ovulación ha ocurrido y dependiendo del valor se tomarán mas muestras de sangre. Todas las muestras deben mantenerse refrigeradas. Enviar los sueros separados, bien señalados y refrigerados para la medición de progesterona.
Interpretación
En valores < 1-3 nmol/L la ovulación no ha ocurrido y se deben tomar muestras en 2-4 días. Valores > 6 nmol/L indican que la ovulación ha ocurrido y se deben tomar mas muestras seriadas. Para valores entre 16-20 nmol/L se debería montar a la perra en 33-57 horas. Para valores entre 20-38 nmol/L se debería montar a la perra en 9-33 horas. Para valores > 38 nmol/L se debería montar en 9 horas.
Protocolo de detección de gestación (progesterona-relaxina)
Indicaciones
Diagnóstico de gestación en perras y gatas y diagnóstico de no gestación en gatas.
Protocolo
Se determinan ambas hormonas en una única muestra.
Interpretación
La perras no gestantes tienen niveles significantes de progesterona como parte de su ciclo normal (metaestro) y por lo tanto la progesterona no puede usarse como indicador de gestación. Después de la gestación la relaxina aumenta hasta niveles detectables hacia los días 21-28. Pueden existir falsos negativos en camadas pequeñas (< 3 cachorros). En gatos, puede usarse la progesterona para indicar que no hay gestación si hay valores < 3 nmol/L. Unos valores altos de relaxina también indican gestación en la gata.
Protocolo para el síndrome de ovario remanente en gatos
Indicaciones
Si existe tejido ovárico como resultado de una ovariohisterectomía incompleta se desarrollarán folículos de forma natural o de forma artificial si administramos FSH. En cualquiera de los casos la ovulación debe inducirse con hCG exógena o GnRH.
Protocolo
Si el animal está en celo inyectar 50-100 UI de hCG vía SC ó 25 mcg de GnRH vía IM. Extraer un muestra sanguínea aproximadamente a los 7-10 días. Si el animal no está en celo o nos encontramos en una situación donde no se pueden esperar los 10 días, hay que inducir el celo. Inyectar 2 mg/día de FSH. Parar el tratamiento cuando el gato muestre signos de celo o después de 5 días (lo que sea más pronto). Seguir con el protocolo anterior. Es mejor la GnRH por el menor riesgo a una reacción anafiláctica. Enviar los sueros separados, bien señalados y refrigerados para la medición de progesterona en ambas muestras.
Interpretación
Una progesteronemia > 1 ng/ml (3,2 nmol/L) indica que existe tejido ovárico. Este protocolo se está sustituyendo por la determinación de LH en una única muestra. Si la LH está baja implica que existe tejido ovárico, y si está alta indica que no hay ovario remanente.
Protocolo para detectar actividad ovárica en perro
Indicaciones
Se usa para detectar si las perras han sido castradas o bien si hay actividad ovárica residual. El protocolo se basa en la estimulación ovárica con la GnRH.
Protocolo
Se extrae la primera muestra basal (T0) y se inyecta 0,32 mg de GnRH vía IV para una perra de 12-15 kg. Esperar 1-2 horas y extraer la segunda muestra. Enviar los sueros separados, bien señalados y refrigerados para la medición de estradiol en ambas muestras.
Interpretación
En machos y en hembras en anoestro la muestra pre-inyección suelen estar < 18 pmol/L. En caso de existir actividad ovárica (hembras sin castrar o con tejido ovárico residual) o actividad testicular anormal en machos, se alcanzan valores de 55-74 pmol/L. Unos niveles > 100 pmol/l en la muestra basal indicarían la presencia de tejido ovárico.
Protocolo de Respuesta a hCG para detectar tejido testicular en machos
Indicaciones
Es un test dinámico para averiguar la presencia de tejido testicular en machos.
Protocolo
Extraer sangre de animal (T0) e inyectar 250 UI de hCG/por animal vía SC ó 2,2 mcg/kg de GnRH vía IM para perros ó 25 mcg por vía IM por gato. Recoger sangre a 1 hora (T1) y 2 horas (T2). Enviar los sueros separados, bien señalados y refrigerados para la medición de testosterona en ambas muestras.
Interpretación
En perros castrados las muestra basal es < 0,5 nmol/L y en la muestra post-estímulo no hay elevación o si la hay es muy ligera. En perros criptórquidos la muestra basal es 3-30 nmol/L y en la muestra post estímulo hay un aumento significativo.
Protocolo de insulinoma
Indicaciones
Para el abordaje diagnóstico del insulinoma.
Protocolo
Esperar o provocar una hipoglucemia. La muestra para insulina debe ser extraída mientras el perro está en hipoglucemia (< 60 mg/dl).
Interpretación
Los valores de insulina en perros en ayunas son menores de 20 mU/ml. Si durante una hipoglucemia la insulina es > 20 mU/ml se considera que hay una secreción excesiva.
Protocolo dinámico de Acidos Biliares
Indicaciones
Diagnóstico de trastornos de funcionalidad y alteraciones en la circulación hepáticas.
Protocolo
Después de 12 horas de ayuno extraer sangre del animal (T0). Administrar comida (2-3 cucharadas soperas de comida de lata de buena calidad para pacientes > 5 kg y 2-3 cucharaditas para pacientes < 5 kg). Extraer otra muestra de sangre a las 2 horas (T1). Tanto hemólisis como lipemia pueden producir resultados erróneos y debe repetirse el protocolo. En pacientes con signos de encefalopatía se deben administrar una comida con restricción de proteína y una pequeña cantidad de aceite vegetal. La contracción de la vesícula biliar también puede ocurrir con excitación y por oler comida, por lo que la contracción puede ocurrir antes de extraer la segunda muestra.
Interpretación
Las determinaciones en ayunas y la de 2 horas post-pandrial, son útiles en la detección de anormalidades de función hepatobiliar o circulatorias. La Especificidad de ACB post-pandriales, llega al 100 % en perro a valores > 35 mcmol/L y en gato a > 30 mcmol/L.
Protocolo de Malasimilación
Indicaciones
Las concentraciones de cobalamina y folatos son útiles en el diagnóstico de la malabsorción o sobrecrecimiento bacteriano (actualmente conocida como diarrea con respuesta a antibióticos).
Protocolo
Valorar Cobalamina y Folatos en una sola muestra. (Mejor si es la misma muestra donde se determina la TLI).
Interpretación
Valores de folatos bajos sugieren una malabsorción de intestino delgado proximal. Niveles de cobalamina bajos sugieren malabsocrión del intestino delgado distal. Niveles de cobalamina bajos o normales junto a niveles de folatos altos sugieren un sobrecrecimiernto bacteriano.
Protocolo de monitorización cardiaca
Indicaciones
Controlar las terapias con digitálicos
Protocolo
Si se medica 1 vez al día extraer la muestra 10−12 horas post−medicación. Si se medica 2 veces al día extraer la muestra 6−8 horas después de la última dosis o inmediatamente antes de la próxima dosis. El estado estacionario se alcanza a los 7−10 días de empezar el tratamiento o de haber efectuado algún ajuste en la dosis.
Interpretación
El rango terapéutico de la Digoxina es de 0,8 − 2.0 ng/ml
Protocolo de monitorización fenobarbital
Indicaciones
Controlar la terapia anticonvulsiva con fenobarbital
Protocolo
El fenobarbital debe administrarse durante 2−3 semanas antes de valorar sus concentraciones. El tiempo de recogida de la muestra post−terapia depende de consideraciones terapéuticas. A las dosis habituales de tratamiento, recomendamos no realizar controles antes de las 3 primeras semanas de tratamiento y a partir de este tiempo extraer una primera muestra a las 4−5 horas (pico de acción, principalmente si se sospecha toxicidad) y otra a las 8−12 horas post−medicación. Monitorizar niveles de Fenobarbital cada 6 meses.
Interpretación
Los niveles terapéuticos son de 15−40 mg/ml
Protocolo de monitorización de Bromuros
Indicaciones
Controlar las terapias con bromuro sódico
Protocolo
La extracción de la muestra respecto al momento de la toma de la medicación no es importante por su larga vida media plasmática. El estado estacionario no se alcanza hasta los 3−4 meses después de empezar el tratamiento o de algún cambio en la dosificación. La valoración del Bromuro debe realizarse a los 30 y 120 días del inicio de la terapia y luego cada 6 meses. En los animales con esta terapia también es importante la valoración del número de las células sanguíneas (Hemograma) cada 6−12 semanas para el control productivo de la médula ósea, y de varios enzimas hepáticos cada 6−12 semanas si hay riesgo de hepato−toxicidad
Interpretación
Los niveles terapéuticos son 0,5 mg/ml.
Aunque la interpretación de los resultados en bioquímica plasmática es bastante específica para cada constituyente en particular, existen unos principios básicos generales que se pueden seguir.
El plasma es básicamente un fluido extracelular en movimiento, que transporta un gran numero de sustancias desde sitios de absorción o producción a sitios de utilización o excreción. Una vez tenemos el resultado contrastado, el primer factor en el que debemos pensar, debe ser si existe alguna razón para que esta sustancia esté en el plasma, es decir si su presencia esta justificada o no. El paso siguiente debe ser saber de donde viene y a donde va esta sustancia, es decir, cuales son los mecanismos responsables de su incorporación y su eliminación del plasma, y el control de dichos mecanismos.
A partir de aquí no nos será difícil empezar a diferenciar las causas de la existencia de concentraciones anormales de cualquier sustancia. Unas concentraciones anormalmente bajas, pueden ser debidas a, bien una incorporación al plasma disminuida ( un deterioro en la síntesis, deficiencia nutricional, pobre absorción, falta de precursores...) o bien a un aumento en su eliminación plasmática ( demanda excesiva, excreción excesiva, perdidas patológicas....). Al contrario, unas concentraciones anormalmente altas, pueden ser debidas bien a un aumento de su incorporación al plasma ( aumento de la producción o de la entrada, liberación patológica del compartimento intracelular...) o bien a una disminución de su eliminación plasmática (disminución de su utilización, excreción impedida...)
Acidos Biliares
Los ácidos biliares (ACB) son sintetizados en hígado a partir del colesterol y se conjugan con taurina o glicina antes de su excreción como sales biliares en la bilis. La acción bacteriana en el intestino deconjuga algunos ácidos biliares. Estos productos entran a la circulación portal y son extraídos y reciclados por los hepatocitos. Si estos ACB no son extraídos son medidos en sangre periférica. La medición de los ACB es un test sensible de función hepática
Tests complementarios: Los niveles de ACB deben determinarse junto a los otros tests de daño hepatocelular o de función hepática como en el perfil hepático
Aumento
- Disminución de la función hepática: Cirrosis, Shunt Portosistémico (congénito o adquirido)
- Colestasis
- Ictericia
ALT
Aumento
Muy específica de hígado. Se encuentra en el citoplasma de los hepatocitos y se libera a circulación durante cambios en la membrana del hepatocito o necrosis. Su localización tan superficial implica que en daños hepáticos moderados (ej. Hipoxia) se puedan producir niveles moderadamente altos en plasma.
Tests complementarios: Los niveles de ALT deben determinarse junto a los otros tests de daño hepatocelular o de función hepática como en el perfil hepático
- Hepatopatías primarias
- Enfermedad hepática aguda
- Hepatitis activa crónica
- Hepatitis tóxica
- Complejo Colangio-hepatitis (f)
- Pancreatitis aguda
- Necrosis hepatocelular
- Neoplasia
- Hígado graso
- Hepatopatías secundarias
- Enfermedades metabólicas: Diabetes Mellitus, Hiperadrenocorticismo
Amilasa
Aumento
Su principal origen es páncreas e intestino delgado. En animales sanos la mayor parte de la amilasa proviene de intestino delgado
Tests complementarios: Debe valorarse junto a la lipasa, un perfil de función renal y TLI
- Origen pancreático
- Inflamación, Neoplasia, Necrosis, Obstrucción conducto pancreático
- Enfermedad intestinal (enteritis, íleos, peritonitis, colecistitis)
- Fallo renal (Disminución filtración)
- Medicaciones: corticoides, glucantime
AST
Aumento
Existe en varios tejidos, pero sus mayores concentraciones están en el músculo esquelético, cardiaco e hígado.
Tests complementarios: Debería determinarse junto a los otros tests de daño hepatocelular o de función hepática como en el perfil hepático
- Enfermedades hepáticas (véase ALT)
- Daño en músculos esqueléticos
- Desórdenes en músculo cardiaco
Bilirrubina
Aumento
Aproximadamente el 80-85 % de la bilirrubina viene de la hemoglobina. La Hemoglobina liberada de los eritrocitos viejos, es fagocitada por el Sistema Fagocítico Mononuclear y se forma Bilirrubina indirecta (BI). Esta BI es liberada a la circulación donde se une a la albúmina y es transportada al hepatocito. Una vez en el hepatocito la bilirrubina sufre la conjugación. Esta conjugación deja a la Bilirrubina susceptible de ser eliminada vía biliar ( Bilirrubina Directa o Conjugada). El proceso continúa a través del sistema biliar extrahepático y hacia intestino donde las bacterias reducen la bilirrubina a urobilinógeno
Tests complementarios: Los niveles de bilirrubina deben determinarse junto a los otros tests de daño hepatocelular o de función hepática como en el perfil hepático.
- Origen prehepático: Enfermedad hemolítica
- Origen hepático
- Colestasis Intrahepática: Cirrosis, Hiperplasia nodular, lipidosis felina, colangitis/colangiohepatitis, Sepsis
- Colestasis Extrahepática: Colangitis, Colecistitis, Colelitiasis, Neoplasia biliar, Pancreatitis
Calcio
Aumento
Disminución
El 99 % del calcio corporal se encuentra en esqueleto y esta en una forma poco utilizable. La mayoría de calcio restante (tisular y no esquelético ) es intracelular en tejido subcutáneo, tendones, músculos…(0.9 %). El Fluido Extracelular, contiene el resto del calcio total, es el calcio sérico y representa el calcio sanguíneo (0.1 %). La medición laboratorial del calcio total debe interpretarse junto con los valores de albúmina y el conocimiento del status ácido-básico del paciente, ya que solo la fracción iónica es activa en procesos como la formación ósea, actividad neuromuscular.
Tests complementarios: Deben realizarse tets del metabolismo fosfocálcico (PTH, fósforo, albúmina) y de función renal (urea, creatinina)
- No Patológica
- Lipemia, cachorros en crecimiento, deshidratación, Hiperproteinemia
- Neoplasia (pseudohiperparatiodismo)
- Linfosarcoma, adenocarcinomas sacos anales, Mieloma
- Hiperparatiroidismo primario
- Hiperparatiroidismo renal secundario
- Hipervitamiosis D
- Sobredosis, rodenticidas de calciferol
- Hemoconcentración
- Hiperadrenocorticismo
- Fallo renal
- Fenómenos de osteolisis
- Osteomielitis, osteoporosis
- Hipoalbuminemia
- Fallo renal crónico con Hiperparatiroidismo renal secundarios
- Eclampsia
- Hipoparatiroidismo primario
- Pancreatitis
- Dietario
- Hipovitaminosis D, exceso de fósforo Hiperparatiroidismo secundario nutricional
- Fallo renal agudo
- Malabasorción intestinal
- Hipomagnesemia
- Intoxicación con etilen glicol
Cloro
Disminución
Aumento
El cloro representa los 2/3 de los aniones existentes en el plasma. Los cambios en el cloro deben interpretarse siempre junto a los cambios en el agua corporal libre, la cual altera las concentraciones de sodio y cloro proporcionalmente y en paralelo. Los cambios observados en las concentraciones de cloro no relacionados con cambios ocurridos en el agua libre o las concentraciones de sodio, están asociados a anormalidades ácido-básicas.
Tests complementarios: Se recomienda medir el cloro junto a los otros electrolitos sodio y potasio y un perfil renal
- Vómito contenido gástrico
- Alcalosis Metabólica
- Deshidratación
- Acidosis metabólica
- Terapia con bromuros
Colesterol
Disminución
Aumento
El Colesterol es el esteroide más común. Es un componente esencial de las membranas celulares y de las vainas de mielina, y es un importante precursor de hormonas esteroideas y sales biliares. Su origen al igual que los triglicéridos puede ser externo o interno. La mayoría de colesterol es sintetizado in vivo en el hígado, y el resto proviene de la dieta.
Tests complementarios: Es importante incluir el colesterol junto a las otras pruebas destinadas a investigar el metabolismo lipídico y triglicéridos.
- Disminución de la absorción
- En problemas de Malaabsorción, Maladigestión (Enteropatía con pérdida proteínas, insuficiencia pancreática exocrina..)
- Disminución de la producción: Shunts Portosistémicos, Fallo hepático
- Colestasis
- Enfermedad endocrina
- Hipotiroidismo, Hiperadrenocorticismo, Diabetes mellitus
- Dietario, Postpandrial
- Medicaciones: corticoides
- Síndrome nefrótico
- Hiperlipidemia primaria: Hipercolesterolemia idiopática, Hiperquilomicronemia primaria (f), Deficiencia de lipoprotein lipasa (f)
Colinesterasa
Disminución
Estas actividades enzimáticas se usan como test diagnóstico en las exposiciones y/o intoxicaciones por organosfosforados o carbamatos. Estos tóxicos son inhibidores de la colinesterasa y por lo tanto la exposición y/o intoxicación disminuye sus valores en sangre.
Intoxicaciones por organofosforados o carbamatos
Creatinina
Disminución
Aumento
La creatinina se forma en el músculo esquelético, es filtrada por los glomérulos, y es excretada por la orina. No es reabsorbida por los túbulos renales. La concentración de creatinina en la sangre es inversamente proporcional a la Tasa de Filtración glomerular.
Tests complementarios: Valorar la urea en el conjunto de un perfil renal y/o muscular
Disminución de la masa muscular
- Azotemia
- Pre-renal, renal o Post-renal
Creatin kinasa (CK)
Aumento
La CK es una enzima. citosólico que existe en grandes cantidades en músculo esquelético y en menor cantidad en miocardio, músculo liso, y encéfalo. En otros órganos su actividad es muy baja e inferior al 5% de su actividad.
Tests complementarios: Valorar la CK junto a AST y creatinina
- Enfermedad muscular inflamatoria
Fibrinógeno
Disminución
Aumento
Se clasifica como Globulina en base a sus características solubles, y contribuye al 3-6 % de las proteínas plasmáticas. Sólo existe en el plasma y no en el suero.
- Fallo hepático
- Coagulopatías
- Hipofibrinogenemia primaria
- Inflamación
- Gestación
Fosfatasa Acalina
Aumento
Los isoenzimas de la ALP se encuentran en una gran variedad de tejidos e incluyen intestino, hígado, hueso, placenta, riñón y leucocitos. Su elevación se debe a un aumento en su síntesis. El isoenzima hepático tiene una vida media de 3 días en perro y 6-8 horas en gato. Los aumentos suelen ser mayores en perro pero tienen mayor significación unos menores aumentos en gatos. Los isoenzimas de origen no hepático tienen poca significación diagnóstica. Los niveles de ALP permanecen elevados durante la reparación del daño hepático, por lo que su elevación nos siempre indica un mal pronóstico.
Tests complementarios: Los niveles de ALP deben determinarse junto a los otros tests de daño hepatocelular o de función hepática como en el perfil hepático.
- Fisiológico
- Crecimiento ©
- Enfermedad hepática
- Colestasis ( Intrahepática o Exrtrahepática)
- Complejo cholangio- hepatitis (f)
- Daño hepático (otras hepatopatías ver ALT)
- Anoxia hepática (anemia)
- No específico
- Drogas ( Glucocorticoides, Fenobarbital..)
- Causa endocrina ( Hiperadrenocorticismo(c), Hipertiroidismo(f), Diabetes Mellitus... )
- Pancreatitis
Tumores óseos
Fructosamina
Disminución
Aumento
La fructosamina mide la glicolización de las proteínas séricas (principalmente la albúmina) y es una medición fiable de la concentración de glucosa en las 1-2 semanas previas
Tests complementarios: Debe medirse junto a la glucosa y a la Insulina
- Hipoproteinemia
- Anemia
- Diabetes mellitus
- Hiperglucemia prolongada (f)
GGT
Disminución
Aumento
Se encuentra en altas concentraciones en hígado y túbulos renales y en menor grado en páncreas e intestino delgado
Tests complementarios: La actividad de la GGT debe determinarse junto a los otros tests de daño hepatocelular o de función hepática como en el perfil hepático.
Hemólisis
- Colestasis Intra o Extrahepática
- Drogas: Glucocorticoides, Anticonvulsivos
Glucosa
Disminución
Aumento
La glucosa es la fuente de energía del cuerpo y se regula por la acción conjunta de insulina y glucagón. La glucosa pasa por el glomérulo renal y se reabsorve en su totalidad en los túbulos. Conforme la glucosa aumenta este mecanismo se satura y se pasa el umbral renal de la glucosa y ésta aparece en la orina.
Tests complementarios: Debe medirse junto a la fructosamina y a la Insulina
- Fallo hepático
- Enfermedad endocrina
- Hipoadrencorticismo, Hipopituitarismo
- Inanición
- Neoplasia
- Hiperinsulinismo: Insulinoma, iatrogénia
- Idiopática: Perros toy, cachorros
- Septicemia
- Policitemia
- Leucemia
- Fisiológica: Postpandrial
- Medicamentos: Cortiocoides, Acetato de megestrol....
- Diabetes mellitus
- Hiperadrenocorticismo
- Acromegalia
- Hipertiroidismo
- Pancreatitis aguda
Hierro
Disminución
Aumento
Aunque la mayoría del hierro corporal se encuentra en los eritrocitos en forma de hemoglobina, existe otra parte del hierro que es almacenada en tejidos, especialmente hígado y bazo. La medición del hierro sérico mide la disponibilidad del hierro en la circulación, pero por si solo no refleja los depósitos de hierro corporal.
Tests complentarios: Deben valorarse otros aspectos del metabolismo del hierro y eritrocitario
- Pérdida crónica de sangre al exterior
- Deficiencia dietaria
- Hemólisis
Lipasa
Aumento
Enzima secretada sólo por el páncreas y la mucosa gástrica solamente y degradada por los riñones. La lipasa hidroliza los triglicéridos.
Tests complementarios: Debe valorarse junto a la amilasa, un perfil de función renal y TLI
- Enfermedad pancreática: Pancreatitis, necrosis
- Neoplasia
- Enteritis
- Enfermedad renal (Azotemia)
- Glucocorticoides
Fósforo
Disminución
Aumento
Aproximadamente el 80-85 % del fósforo total corporal, se encuentra en el hueso, mientras que el 15 -20 % esta en tejidos blandos como los músculos. La absorción neta del fósforo es aproximadamente 60-70 % de la carga ingerida. Esta absorción está disminuida por bajos niveles de Vitamina D y niveles altos de calcio y bajos de fósforo en la dieta, y aumentada por bajos niveles dietarios de calcio, aumento de la acidez de la dieta, la hormona de crecimiento y la Vitamina D. El fósforo se excreta en saliva heces (30-40 %) y orina (60-90 %). El 80-90 % del fósforo filtrado sufre reabsorción tubular.
Tests complementarios: Deben realizarse tets del metabolismo fosfocálcico (PTH, fósforo, albúmina) y de función renal (urea, creatinina)
- Hiperparatiroidismo: Primario, renal secundario
- Neoplasia: Hormona PTH-like, tumores tiroides
- Insulinoterapia
- Cetoacidosis diabética
- Deficiencia dietaria
- Eclampsia
- Hiperadrenocorticismo
- Fallo renal agudo o crónico
- Azotemia Postrenal
- Hemólisis
- Hipertiroidismo
- Neonatos
- Hipervitaminosis D
- Hipoparatirodismo
- Exceso dietario
- Osteolisis
Potasio
Disminución
Aumento
El Potasio es el catión más abundante que existe en el organismo. Su concentración sérica no es un buen reflejo del contenido total ya que aproximadamente el 98 % del potasio corporal es intracelular, y solo el 1-2 % es extracelular. El Potasio sérico esta gobernado por un balance externo existente entre su toma diaria y su eliminación diaria vía renal ( Regulación Renal ), y por un balance interno de redistribución entre los diferentes sectores hídricos del organismo (Regulación Extrarenal ).
Tests complementarios: Se recomienda medir el potasio junto a los otros electrolitos sodio y cloro y un perfil renal
- Alcalosis
- Deficiencia dietaria (gatos)
- Pérdida Fluidos Gastrointestinales
-Hiperadrenocorticismo
- Hiperaldosterenismo
- Insulinoterapia
- Trastorno renal:
- Diuresis post-obstructiva, Acidosis tubular renal, fallo renal poliúrico
- Fallo renal oligúrico-anúrico
- Obstrucciones y/o rotura tracto urinario
- Hipoadrenocorticismo
- Acidosis metabólica
Proteínas totales
Disminución
Aumento
El Plasma, contiene muchas proteínas diferentes y cada una con funciones diferentes. Estas Proteínas, se clasifican en Albúminas, Alfa-Globulinas, Beta-Globulinas y Gamma-Globulinas. La mayoría de estas Proteínas Plasmáticas son sintetizadas en el hígado excepto las Inmunoglobulinas, que son sintetizadas en el Sistema Reticuloendotelial.
Tests compelemntarios: Parámetro imrescindible en todos los perfiles bioquímicos.
- Hemorragias
- Pérdida gastrointestinal: Enteropatía con pérdida porteíca (albúmina y globulinas)
- Hipoalbuminemia
- Fallo hepático: Atrofia, Fibrosis, Cirrosis, Shunts PS
- Pérdida renal: Glomérulonefritis, Amiloidosis
- Malasimilación: Malabsorción, Maladigestión,
- Enfermedades exudativas cutáneas graves
- Mala nutrición
- Efusiones crónicas,
- Hipoglobulinemia
- Neonatos
Inmunodeficiencias: Congénitas o adquiridas
- Deshidratación (albúmina y globulinas)
- Hiperglobulinemia
- Inflamación
- Gamapatía Policlonal
- Enfermedad inflamatoria crónica, PIF, Dermatitis, Enfermedad inflamatoria intestinal, Enfermedades infecciosas/ parasitarias (leishmaniosis, ehrlichiosis), enfermedades inmunomediadas, neoplasias
- Gamapatia Monoclonal
- Mieloma., Ehrlichia, Diroflariosis
- Error laboratroio
- Hemólisis, Lipemia
Hiperalbuminemia (Error laboratorio)
Sodio
Disminución
Aumento
Existe principalmente en fluido extracelular y es el pricnipal contribuyente de su osmolaridad. La cantidad de sodio, y con él la cantidad de agua, es regulada por el riñón que mantiene sus concentraciones a pesar de la ingesta de agua.
Tests complementarios: Se recomienda medir el sodio junto a los otros electrolitos cloro y potasio y un perfil renal
- Hipoadrencorticismo
- Diabtes mellitus
- Pérdida fluidos gastrointestinales
- Efusiones crónicas
- Exceso de ADH
- Diuréticos
- Administración de fluidos hipotónicos
- Polidipsia psicogénica
- Fallo renal poliúrico
- Hiperaldosterensimo
- Pérdida de fluidos intestinales
- Diabetes Insípeda
- Fallo renal
- Deshidratación
- Pérdida insensible de fluidos
- Disminución ingesta de agua
- Aumento en la ingesta de sal
Troponina I
Aumento
Es una proteína del músculo cardiaco (cTnI). Muy útil para el diagnóstico precoz de la lesión del miocardio ya que es liberada a la circulación muy poco tiempo (4 a 5 horas) después de una lesión miocárdica y persiste en plasma durante, al menos, 7 a 9 días.
Tests complementraios: Es recomendable medio otros marcadores cardíacos como la ET1 y pro ANP.
Enfermedades de origen cardíaco que afecten al miocardio
Urea
Disminución
Aumento
La urea es una sustancia nitrogenada no proteica que se sintetiza en el hígado como mecanismo de excreción del amonio generado por el catabolismo de los compuestos que contienen nitrógeno (aminoácidos dietarios y endógenos). Es filtrada por el glomérulo y reabsorbida por los túbulos de forma que menos del 50 % de la urea filtrada por el glomerulo aparece en la orina final. La concentración de urea en la sangre es inversamente proporcional a la Tasa de Filtración Glomerular (TFG).
Tests complementarios: Valorar la urea en el conjunto de un perfil renal y/o hepático
-Enfermedad hepática avanzada
- Diuresis
- Caquexia
- Insuficiencia renal
- Aumentos moderados en
- Hemorragia intestinal, bacterias entéricas
El Urianálisis completo, consiste en la evaluación de las propiedades físico-químicas de la orina, la estimación de la concentración de sus solutos, y el examen microscópico del sedimento. Indicado tanto en pacientes con sospecha de enfermedad del sistema urinario como en pacientes con desordenes no urinarios, ya que aporta información de varios sistemas corporales. Como casi todos los tests laboratoriales, los resultados del Urianálisis son validos pero no infalibles, y su valor diagnostico es directamente proporcional a la capacidad que se tenga para interpretarlos.
|
Volumen · Normal: 25-30 ml/kg/día |
||
| Color · Normal: amarillo o ámbar | ||
El color normal de la orina es amarillo o ámbar y se debe fundamentalmente a la presencia de dos pigmentos: urocromos y urobilina. Un color amarillo oscuro, normalmente indica que la orina está concentrada, si la orina es diluida el color es amarillo muy claro, por ello el color debe ser interpretado junto a la DU. El color de la orina puede variar por diversas causas, y puede producirse tanto por pigmentos exógenos como endógenos. |
|
|
|
Turbidez · Normal: transparente |
||
| Cuando la orina está muy concentrada tiene más posibilidad de ser turbia que si la orina está diluida. Cambios en la temperatura y pH pueden producir pérdida de transparencia. Normalmente las causas que pueden producir turbidez en la orina pueden ser determinadas examinando el sedimento urinario. | Causas de Turbidez
|
|
|
Densidad · Dependiendo de las necesidades de agua y/o solutos del organismo, cualquier valor comprendido entre 1.001 y 1.065 o más en perros y entre 1.001 y 1.080 en gatos, puede ser normal. |
||
| La DU se usa para determinar la capacidad de los túbulos renales para concentrar o diluir la orina. Dependiendo de las necesidades hídricas del animal, el riñón puede producir orina que será muy concentrada o muy diluida. Cuando el agua está en exceso, hay una mayor reabsorción de solutos que de agua, y se produce una orina diluida aumentando su volumen. Cuando hay carencia de agua ocurre el proceso contrario, hay una mayor reabsorción de agua que de solutos, y se produce una orina muy concentrada. | Isostenuria
|
Hipostenuria
|
|
Glucosa · Valor Normal: negativo |
||
| La glucosa que se encuentra en plasma atraviesa libremente el capilar glomerular, aparece en el filtrado glomerular, y se reabsorbe casi en su totalidad de forma activa en túbulos proximales, de manera, que sólo una mínima cantidad (2-10 mg/dl) aparece en orina. | Positivo
|
|
|
Bilirrubina · Valor Normal: 0-2+ |
||
| La bilirrubinuria se produce cuando aumenta la concentración de bilirrubina conjugada en el plasma. | Positivo
|
|
| Cetonas · Valor Normal: Negativo | ||
Normalmente se forman pequeñas cantidades de cuerpos cetónicos que, en cantidad limitada, son metabolizados por los tejidos periféricos. En pequeña proporción son filtrados por los glomérulos y reabsorbidos completamente por los túbulos renales. |
|
|
|
Sangre · Valor Normal: Negativo |
||
| El test se basa en la actividad de la seudoperoxidasa que contiene el grupo hemo, presente tanto en la hemoglobina como en la mioglobina. La reacción es más sensible cuando existe pigmento libre que cuando se localiza en el interior de los hematíes. Con este test es posible detectar la presencia de hematuria antes de que se manifieste de forma macroscópica. | Positivo
|
|
|
Ph |
||
| Es la medición de la concentración de H+. Un pH de 7 se considera neutro, mientras que un valor más alto (7.1- 14) es alcalino, y un valor más bajo (0-6.9) es ácido. | Disminución
|
Aumento
Dietario |
|
Proteínas · Valor Normal: Negativo-1+ (depende DU) |
||
| Pequeñas cantidades de proteínas pasan a través del filtrado glomerular y después son reabsorbidas por los túbulos. Las proteínas que pueden aparecer en la orina (proteinuria) son una mezcla de cantidades variables de proteínas plasmáticas, proteínas originadas en el tracto urinario y, dependiendo del método de recogida de la orina, proteínas del tracto genital. | Enfermedad glomerular
Enfermedad inflamatoria
|
|
| Leucocitos · Valor Normal: 0-2. Si la orina es recogida mediante cistocentesis es normal encontrar hasta 5 leucocitos/campo (x40) | ||
En orinas frescas aparecen como células esféricas 1,5 veces mayor que los eritrocitos y más pequeños que las células del epitelio de transición. Son difíciles de diferenciar de las células epiteliales de los túbulos renales. Los leucocitos se lisan si la orina es alcalina o hipostenúrica. |
|
|
| Hematíes · Valor Normal: 3-8 eritrocitos/campo (x40) dependiendo del método de recogida | ||
En orinas frescas se observan en forma de disco bicóncavo y coloración pálida, más pequeños que los leucocitos y sin núcleo. Si han estado tiempo en la orina se observan sin color ya que pierden la hemoglobina. En orinas muy concentradas aparecen crenados y con formas anómalas, y en orinas diluidas se hinchan y se ven con formas redondeadas. |
|
|
|
|
||
|
La presencia de bacterias en orina (bacteriuria) puede tener, o no, significado patológico, dependiendo del método de recogida de la orina y del tiempo transcurrido hasta que se realiza el análisis. Si la orina es recogida mediante cistocentesis no hay bacterias en una orina normal, pero si es recogida mediante micción o por cateterización, es posible hallar bacterias que contaminan la uretra distal o el tracto genital. |
Contaminación |
|
|
Células epiteliales · Valor Normal: Escasas |
||
| En animales sanos es normal hallar algunas células epiteliales, tanto las del epitelio renal, del epitelio de transición de la pelvis renal, uréteres, vejiga y uretra, como células escamosas de la vagina y uretra distal. | Aumento
|
|
|
Cilindros · Valor Normal: ausencia o muy escasos granulosos |
||
| Los cilindros son estructuras constituidos por células o proteínas moldeadas en los túbulos renales. Básicamente, están compuestos por la mucoproteína de Tamm-Horsfall. Esta mucoproteína la secretan las células epiteliales de las asas de Henle, de los túbulos distales y de los túbulos colectores, lugares donde se forman los cilindros. | Aumento
|
|
La Hematología, es básicamente una técnica de screening que se usa normalmente junto a otros tipos de investigaciones laboratoriales, y su importancia diagnóstica variará según cada caso. La hematología tiene dos propósitos fundamentales, confirmar el diagnóstico de enfermedades sanguíneas específicas, y servir de ayuda en el diagnóstico de condiciones que no son de origen hematológico, pero que causan cambios no específicos pero apreciables en la distribución de las células sanguíneas.
| GLÓBULOS BLANCOS | Disminución | Aumento |
Disminución de producción
Consumo excesivo
Secuestro
|
Infección Inflamación Enf inmunomediada Trauma tisular extenso Neoplasia Necrosis Leucocitosis fisiológica Estrés Glucocorticoides Leucemia Si asociado a AR
|
|
GLÓBULOS ROJOS |
Disminución |
Aumento |
Anemias regenerativas
Trauma Microangiopáticas Anemias no regenerativas Fallo Renal
Anemia aplásica idiopática |
Deshidratación Policitemia Excitación Hipertiroidismo (f) |
|
PLAQUETAS |
Diminución |
Aumento |
Disminución de la producción en M.O.
Aumento de la destrucción
Pérdida o distribución excesiva
|
Excitación, ejercicio, Traumas Posthemorragias Post esplenectomía Deficiencia de hierro Trastornos mieloproliferativos Infecciones o inflamaciones |
Aunque ciertos trastornos de la Hemostasis puedan requerir el uso de un único test, siempre que sea posible, se debe realizar un perfil de 2-3 pruebas, frente a un problema de hemorragias espontaneas y/o prolongadas, ya que muchos de estos trastornos, pueden cambiar rápidamente y/o afectar a varias áreas del sistema hemostático. La evaluación de uno o dos tests individuales, puede no abordar el defecto hemostático en toda su extensión, o llevar a conclusiones erróneas.
| TPTA (Tiempo Parcial de Tromboplastina Activada) | Prolongado |
Valora la Vía Intrínseca de la coagulación (factores VIII, IX, XI, XII) la Vía Común (factores V, X, II, y fibrinógeno). Se usa como screennig de todos los factores excepto el factor VII. |
|
| TP (Tiempo de Protrombina) | Prolongado |
Valora la Vía Extrínseca de la coagulación (factor VII) y la Vía Común (factores V, X, II, y fibrinógeno). |
|
| TT (Tiempo de Trombina) | Prolongado |
Valora la Fibrinoformación excepto el F XIII. Es independiente de los factores de las otras vias. Depende exclusivamente de la cantidad y funcionalidad del Fibrinogeno y de la presencia de anticoagulantes circulantes. (Heparina, PDFs, y paraproteinas). |
|
| PDFs (Productos de degradación del fibrinógeno) | Aumento |
| La acción de la Plasmina sobre el Fibrinógeno y/o Fibrina (Fibrinolisis) da lugar a la formación de los PDFs. En circunstancias normales, la Fibrinolisis es un proceso controlado que produce una digestión local del trombo. | Fibrinolisis activa sistémica primaria o secundaria (C.I.D.) |
D-Dímeros |
Aumento |
| Se forman por la acción de la plasmina en polímeros de fibrina. Son indicativos de coagulación activa o generación de trombina, y de fibrinolisis (generación de plasmina). | Indican le presencia de tromboembolismo |
Las interferencias en los resultados bioquímicos dependen en gran parte de la metodología usada (analizador y técnica analítica) y de la cantidad de sustancia interferente existente. Por lo tanto estas guías de interferencia deberían considerarse como orientativas y no categóricas. Las principales interferencias son debidas a hemólisis y lipemia.
Hemólisis
Es la liberación de la Hemoglobina del interior del eritrocito. Muchas veces no es aparente hasta que la muestra se ha centrifugado.
| CAUSAS | ||
| Naturaleza in vitro | Naturaleza in vivo | |
|
Mala técnica de venipunción |
Ciertas anemias hemolíticas | |
| Mecanismos por los que la hemólisis afecta algunos resultados | ||
| Mecanismo | Tests afectados | Sentido alteración |
| Liberación de algunos constituyentes a plasma o suero | LDH, AST, Potasio, CK, ALT, Fósforo | Aumento |
| Dilución de constituyentes en el suero | Sodio, Cloro | Disminución |
| Interferencia directa con el color (espectrofotometría) | Bilirrubina Total, Prot.Totales, AST, CK, Albúmina, Lipasa, ALP, Calcio, Creatinina | Variable |
| Aumento de la turbidez (refractometría) | Fibrinógeno, Proteínas plasmáticas | Aumento |
| Interacción química con el analito | Co2, Insulina | Disminución |
Lipemia
Es causada por un aumento de triglicéridos en forma de quilomicrones o lipoproteínas grandes (VLDL) e interfiere en los tests bioquímicos.
| Tests afectados por lipemia | |
| Ensayos punto final (falso aumento) | Ensayos cineticos (falsa disminución) |
| Proteínas totales Bilirrubina Total Albúmina Glucosa Calcio Fósforo Acidos biliares |
Lipasa ALT AST ALP Amilasa |
Ofrecemos la tabla de conversión de unidades de los parámetros más comunes. Ejemplo para convertir un valor de cortisol de 5 g/dl a nmol/L hay que multiplicar x 27.6, es decir 5 g/dl x 27.6 = 138 nmol/L. En el caso de la T4, 20 nmol/L x 0,078 = 1,56 g/dl
| Conversión a UI o valores en ambas unidades | ||||
Parámetro |
Unid.(conv.) |
Unid. (SI) |
Conv.#SI |
SI#conv. |
| Ácido Acetil Salicílico | ug/ml | mmol/l | x 7.25 | x 0.138 |
| Ácido Ascórbico | mg/dl | umol/l | x 56.78 | x 0.0176 |
| Ácido Fólico | ug/dl | nmol/l | x 22.655 | x 0.0441 |
| Ácido úrico | mg/dl | umol/l | x 59.48 | x 0.0168 |
| ACTH | ng/l | pmol/l | x 0.2202 | x 4.5410 |
| Adrenalina | ng/l | pmol/l | x 5.4582 | x 0.1832 |
| Albúmina | g/dl | g/l | x 10 | x 0.1 |
| Aldosterona | ng/dl | pmol/l | x 27.743 | x 0.03605 |
| Amonio | ug/dl | umol/l | x 0.587 | x 1.703 |
| Bilirrubina | mg/dl | umol/l | x 17.104 | x 0.0585 |
| Bun | mg/dl | mmol/l | x 0.3651 | x 2.808 |
| Calcio | mg/dl | mmol/l | x 0.2495 | x 4.008 |
| Calcitonina | g/l | mmol/l | x 0.292 | x 3.42 |
| Cloro | mg/dl | mmol/l | x 0.2821 | x 3.5453 |
| Cobre | ug/dl | umol/l | x 0.1574 | x 6.3532 |
| Colesterol | mg/dl | mmol/l | x 0.026 | x 38.66 |
| Cortisol | ug/dl | nmol/l | x 27.6 | x 0.036 |
| Creatinina | mg/dl | umol/l | x 88.402 | x 0.0113 |
| Digoxina | ug/l | nmol/l | x 1.28 | x 0.781 |
| Estradiol | ug/dl | nmol/l | x 0.34675 | x 0.02884 |
| Fenobarbital | mg/l | mol/l | x 4.31 | x 0.232 |
| Fibrinógeno | mg/dl | g/l | x 0.01 | x 100 |
| Fósforo | mg/dl | mmol/l | x 0.3229 | x 3.0974 |
| Fructosamina | mg/dl | mmol/l | x 0.0555 | x 18.016 |
| Glucosa | mg/dl | mmol/l | x 0.555 | x 18.016 |
| Hemoglobina | g/dl | mmol/l | x 0.620 | x 1.611 |
| Hierro | ug/dl | umol/l | x 0.1791 | x 5.5847 |
| Insulina | ug/l | pmol/l | x 172.1 | x 0.0058 |
| Lactato | mg/dl | mmol/l | x 0.111 | x 9.008 |
| Magnesio | mg/dl | mmol/l | x 0.4113 | x 2.4312 |
| Noradrenalina | ug/dl | nmol/l | x 0.059109 | x 16.95 |
| Plomo | ug/dl | umol/l | x 0.0483 | x 20.719 |
| Potasio | mg/dl | mmol/l | x 0.2557 | x 3.9102 |
| Primidona | mg/l | umol/l | x 4.58 | x 0.218 |
| Progesterona | ng/ml | nmol/l | x 3.18 | x 0.314 |
| Proteinas totales | g/dl | g/l | x 10 | x 0.1 |
| Sodio | mg/dl | mmol/l | x 0.435 | x 2.2989 |
| T3 | ng/ml | nmol/l | x 1.536 | x 0.651 |
| T3 libre | pg/ml | pmol/l | x 1.536 | x 0.651 |
| T4 | ug/dl | nmol/l | x 12.87 | x 0.078 |
| T4 libre | ng/dl | pmol/l | x 12.87 | x 0.078 |
| Testosterona | ng/ml | nmol/l | x 3.47 | x 0.288 |
| Triglicéridos | mg/dl | mmol/l | x 0.0114 | x 87.5 |
| Urea | mg/dl | mmol/l | x 0.1665 | x 6.006 |
| Vitamina A | ug/dl | umol/l | x 0.0349 | x 28.646 |
| Vitamina B12 | ng/dl | umol/l | x 0.7378 | x 1.3554 |
| Vitamina C | mg/dl | umol/l | x 56.776 | x 0.0176 |
| Zinc | ug/dl | umol/l | x 0.153 | x 6.537 |
| Prueba | Valores referencia | Tipo | Condic. de | |
| Perro | Gatos | Muestra | conservac. | |
| Aceticolinesterasa eritrocitaria | 20-40 Ul/gHb | 20-40 Ul/gHb | E | R |
| Acetilcolina, anticuerpos receptores | < 0.68 nM/L | * | S | R |
| Ácido úrico | 0-0.6 mg/dl | 0-0.2 mg/dl | S | R |
| Ácidos biliares (1 det) | < 10 umol/l | < 25 umol/l | S | R |
| Ácidos biliares (2 det) | < 6 umol/l | < 20 umol/l | S | R |
| ACTH (Hormona adrenocorticotropa) | 15-60 pg/ml | 4-40 pg/ml | P | C |
| Albúmina | 2.3-4.5 gr/dl | 2.4-4.0 gr/dl | S | R |
| Aldolasa | 3.5-11 U/L | 3.5-11.1 U/L | S | R |
| Aldosterona | 15-344 pg/ml | 50-139 pg/ml | S/O | LAB |
| ALFA-1 proteasa fecal, inhibidor | 0,23-5,67 mcg/gr | * | H | LAB |
| ALT (Alanin transferasa) | < 100 Ul/L | < 80 Ul/L | S | R |
| Amilasa | 360-1580 U/L | 570-1820 U/L | S | R |
| Antitrombina III | 85-120% | 85-120% | C | R |
| AST (Aspartato aminotransferasa) | < 109 UI/L | < 90 UI/L | S | R |
| Bilirubina | < 0,6 mg/dl | < 0.3 mg/dl | S | R |
| Calcio | 8.7-12.1 mg/dl | 8.3-11.8 mg/dl | S | R |
| Calcio ioinco | 4-4.8 mg/dl | 4-4.8 mg/dl | S | C |
| Calcio, fraccion de excrecion | 0-0.4% | 0-0.4% | O | R |
| Ceruloplasmina | 25-67 mg/dl | 25-67 mg/dl | S | R |
| Ciclosporina | 180 - 600 ng/ml | * | S | LAB |
| Cistatina C | < 3 mg/L | < 3 mg/L | S | R |
| Cloro | 105-117 mEq/L | 116-123 mEq/L | S | R |
| Cloro, fraccion de excrecion | 0-1.0% | 0-1.0% | O | R |
| Cobalamina (VIT. B12) | 150-580 ng/L | 150-1700 ng/L | S | R |
| Colesterol | 125-280 mg/dl | 90-200 mg/dl | S | R |
| Colinesterasa | 4800-12000 U/l | 2200-6500 U/l | S | R |
| Cortisol | 0.5-5.5 ug/dl | 1-4.5 ug/dl | S | R |
| Creatinina | 0.5-1.9 mg/dl | 0.5-2.0 mg/dl | S | R |
| Creatinquinasa | < 120 Ul/L | < 120 Ul/L | S | R |
| Digoxina | 1-2.5 ng/ml | 0.8-2.0 ng/ml | S | R |
| Dimeros -D | < 250 ng/ml | < 250 ng/ml | C | R |
| Endotelina 1 | 0,4 - 1,1 fmol/ml | 0,4 - 1,1 fmol/ml | S | R |
| Enzima convertidor de la angiotensina | 8-45 U/L | 8-45 U/L | S | LAB |
| Eritropoietina | 5-35 mU/ml | 3-39 mU/,l | S | LAB |
| Estradiol | Se comenta en el informe | Se comenta en el informe | S | R |
| Factor de Von Willebrand | 70-180% | * | C | C |
| Fenobarbital | 15-45 g/ml | 15-45 g/ml | S | R |
| Fetoproteina Alfa-1 | 13.3-77.4 ng/ml | * | S | R |
| Fibrinogeno | 150-350 mg/dl | 90-375 mg/dl | C | R |
| Folatos | 4-13 ng/ml | 12-20 ng/ml | S | R |
| Fosfatasa alcalina | < 180 Ul/L | < 180 Ul/L | S | R |
| Fósforo | 2.9-6.5 mg/dl | 3.1-6.8 mg/dl | S | R |
| Fósforo, fracción de excreción | 3-44% | 3-44% | O | R |
| Fructosamina | 187-386 mmol/l | 175-400 mmol/l | S | R |
| Gamma glutamil transpeptidasa (GGT) | < 10 Ul/l | < 11 Ul/l | S | R |
| Gastrina | < 183 pg/ml | < 123 pg/ml | S | LAB |
| GH (Hormona del crecimiento) | 2-5 ug/l | 2.1-6.0 ug/l | S | LAB |
| GLDH | < 10 Ul/L | < 12 Ul/L | S | R |
| Globulinas | 2.5-4.4 mg/dl | 2.6-5 mg/dl | S | R |
| Glucosa | 60-120 mg/dl | 75-160 mg/dl | S | R |
| Glucosa -6-fosfato deshidrogenasa | 100-180 U/10 eritrocitos | * | E | R |
| Haptoglobina | 30-250 mg/dl | 30-250 mg/dl | S | R |
| Hemoglobina glicosilada A1C | < 5% | < 2% | E | R |
| Hidroxibutirato, BETA | 0,0 - 0,32 mmol/L | 0,0 - 0,21 mmol/L | S | R |
| Hierro | 71-185 ug/dl | 70-189 ug/dl | S | R |
| Inmunoglobulina A | 0.4-1.6 mg/ml | 0.35-6.0 mg/ml | S | R |
| Inmunoglobulina G | 10-20 mg/ml | 5.67-38.0 mg/ml | S | R |
| Inmunoglobulina M | 1.0-2.0 mg/ml | 0.7-3.6 mg/ml | S | R |
| Insulina | 5-25 Ul/ml | 4-15 Ul/ml | S | R |
| LH (Hormona luteinizante) | Se comenta en el informe | Se comenta en el informe | S | R |
| Lipasa | < 600 Ul/L | < 175 Ul/L | S | R |
| Lisozima | 0.2-0.8 ug/ml | 0.2-0.8 ug/ml | S/O | R |
| Magnesio | 1.8-2.4 mg/dl | 2.0-2.5 mg7dl | S | R |
| Metahemoglobina | < 1.5% de hemoglobina total | E | R | |
| Osmolalidad | 289-313 mOsmol/Kg | 299-327 mOsmol/Kg | S/O | R |
| Osteocalcina | 2.7-12.3 ng/ml | * | S | R |
| Parathormona intacta | 18-102 pg/ml (2-11 pM) | 0-41 pg/ml (0-4 pM) | S | C |
| Piruvato kinasa | 60-220 U/10 eritrocitos | * | HE | R |
| Plomo | < 20 ug/dl | < 20 ug/dl | E | R |
| Potasio | 3.5-5.6 mEq/L | 3.4-5.6 mEq/L | S | R |
| Potasio, fraccionado de excreción | 0-19% | 0-19% | S/O | R |
| Productos de degradación del fibrinógeno | < 10 ug/ml | < 10 ug/ml | C | R |
| Progesterona | Se comenta en el informe | Se comenta en el informe | S | R |
| Prolactina | 4-35 ng/ml | * | S | R |
| Proteina C reactiva | < 10 mg/L | * | S | R |
| Proteinas | 5.2-7.6 g/dl | 5.5-7.9 g/dl | S | R |
| PTHrP (PTH Related protein) | < 2 pM | < 2 pM | S | C |
| Ratio Ca:P | < 60 | < 60 | S | R |
| Ratio calcio/Creatinina en orina | 0.5-2.3 x10 -2 | 0.5-2.3 x10 -2 | O | R |
| Ratio cortisol/Creatinina en orina | 1.2x 10 -5 | 1.2x 10 -5 | O | R |
| Ratio proteínas/creatinina en o"ria | "< 0,2 Normal; 0.2-1 cuestionable > 1 Anormal" | "< 0.6 normal; 0.6-1 cuestionable > 1 anormal" | O | R |
| Relaxina | Se comenta en el informe | Se comenta en el informe | S | R |
| Sodio | 142-152 mEq/L | 146-160 mEq/L | S | R |
| Sodio, fracción de excreción | 0-0.9% | 0-0.9% | S/O | R |
| Somatomedina C | 200-800 ng/ml | 200-800 ng/ml | S | R |
| T3 (Triyodotironina) | 1.0-2.0 ng/ml | 0.3-0.9 ng/ml | S | R |
| T4 Libre (Tiroxina libre) | 0.4-1.0 ng/dl | 0,5-1,9 ng/dl | S | R |
| T4 Total (Tiroxina total) | 0.8-2.1 g/dl | 1.1-3.2 g/dl | S | R |
| Taurina | 80-100 nmol/mL | 50-100 nmol/mL | S | C |
| Testosterona | 0.5-7 | 0.5-7 | S | R |
| Tiempo de cefalina activada | 10.1-13.5 segundos | 10.1-13.5 segundos | C | R |
| Tiempo de protombina | 5.9-9.8 segundos | 7.6-12.4 segundos | C | R |
| Tiempo de trombina | 11.6-15.7 segundos | 11.6-15.7 segundos | C | R |
| Tiroglobulina, autoanticuerpos | < 2 | * | S | R |
| TLI | 5-25 ug/L | 17-49 ug/L | S | R |
| Triglicéridos | 20-200 mg/dl | 45-150 mg/dl | S | R |
| Troponina I | < 0,2 ng/ml | < 0,2 ng/ml | S | R |
| TSH canina | 0.03-0.6 ng/ml | * | S | R |
| Urea | 18-40 mg/dl | 17-39 mg/dl | S | R |
| Vasopresina | < 6 pg/ml | < 6 pg/ml | S | LAB |
| Vitamina D 1.25 Dihidroxicolecalciferol | 27-42 pg/ml (cachorro aprox.12 semanas: 77-105) | 25-33 pg/ml (cachorro aprox.12 semanas: 32-69) | S | LAB |
Tipo de muestra
C:Citrato; E: EDTA; HE: Heparina; O: Orina; P: Plasma; S: Suero; S/O: Suero o Orina
Conservación
C: Congelación; LAB: Consultar LAB; R: Refrigeración
 |
 | ||
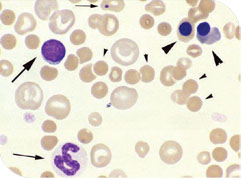
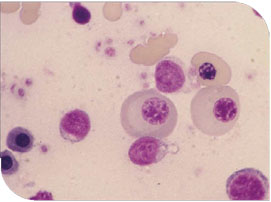
| Frotis Sangre de perro con Anemia Hemolítica Inmunomediada. 1: Metarrrubricitos; 2: Cuerpo de Howell Joly; 3: Esfecrocitos |
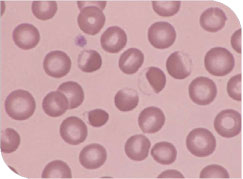
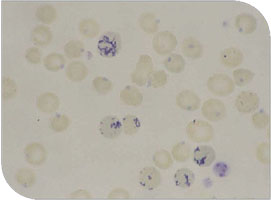
Eccentrocitos en frotis de perro | ||
 |
 | ||
| Frotis sangre de gato con FeLV. Eritrocitos nucleados en el centro con cromatina nuclear inmadura y citoplasma bien hemoglobinizados. |
Cuerpos de heinz en frotis de gato. | ||
 |
 | ||
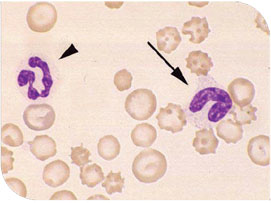
| Neutrófilo cayado y neutrófilo segmentado en sangre de perro |
Demodex Canis | ||
 |
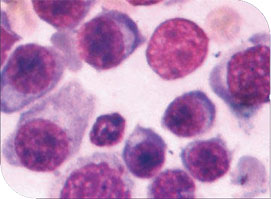 | ||
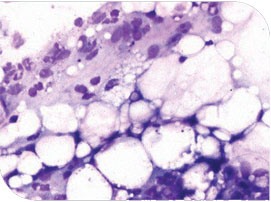
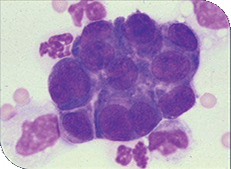
| Hipoplasia de médula ósea en gato | Citología de médula ósea en perro con Mieloma.Plasmocitos en médula ósea. | ||
 |
 | ||
| Células mesoteliales reactivas en citología de efusión. |
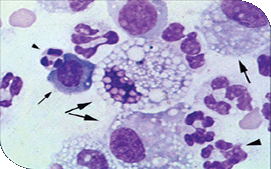
Macrófagos vacuolizados y neutrófilos degenerados en citología de peritonitis | ||
 |
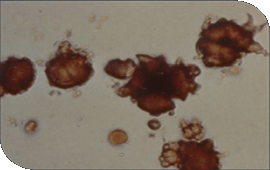 | ||
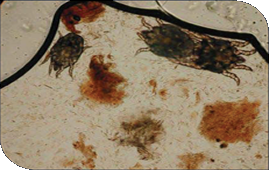
| Otodectes Cynotis | Cristales de biurato amónico en sedimento urinario de perros | ||
 |
 | ||
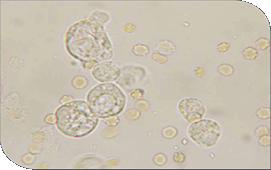
| Células epiteliales de transición en sedimento urinario de perro. |
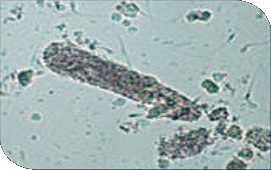
Cilindro granuloso en sedimento urinario de perro | ||
 |
 | ||
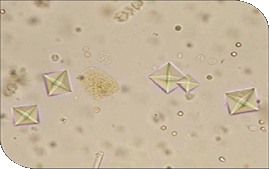
| Cristales de oxalato cálcico en sedimento urinario de gato |
Cristales de estruvita en sedimento urinario de gato. | ||
 |
 | ||
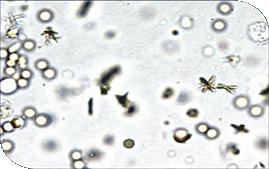
| Cristales de bilirrubina en sedimento urinario de gato |
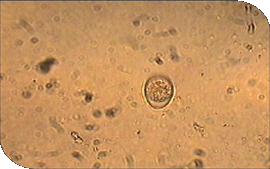
Eimeria spp en flotación de heces de perro | ||
 |
 | ||
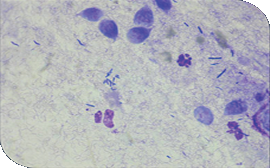
| Trofozoitos de Giardia en examen directo de heces de perro. Tinción dif quick. |
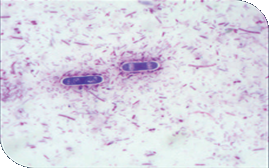
Saccaromycopsis Guttulatus en heces de perro. Tinción diff quick |


